یک هالو اسید است که از قرار گیری اتم هیدروژن در کنار اتم کلر تشکیل شده، اسید کلریدریک (Hydrochloric acid) نام دارد. این ترکیب در دسته مهم ترین مواد صنعتی قرار دارد و با نام آیوپاک کلران شناخته می شود. از مهم ترین کاربردهای آن می توان به خالص سازی فولاد و فلزات دیگر، از بین بردن زنگ زدگی آهن، تولید ترکیبات معدنی، کمک به خنثی سازی و کنترل pH در صنایع، در صنایع رزین، کاربردهای آزمایشگاهی و بسیاری از موارد دیگر می توان اشاره کرد.
خرید هیدروکلریک اسید
برای خرید جزئی اسید کلریدریک و انواع مواد شیمیایی صنعتی دیگر با کیفیت بالا و قیمت مناسب از شیمی استور با مشاوران مجرب ما در واحد فروش تماس بگیرید.
اسید کلریدریک چیست؟
این ترکیب اسیدی قوی با فرمول شیمیایی HCl بوده و به صورت مایعی بی رنگ و شفاف با بویی تیز موجود است. به علت خورندگی بسیار زیادی که دارد کمتر به صورت خالص موجود است و بیشترین کاربرد آن به شکل محلول ۳۷٪ است. این ترکیب به علت داشتن یک پروتون در ساختار خود، در دسته اسیدهای برونشتد قرار دارد.
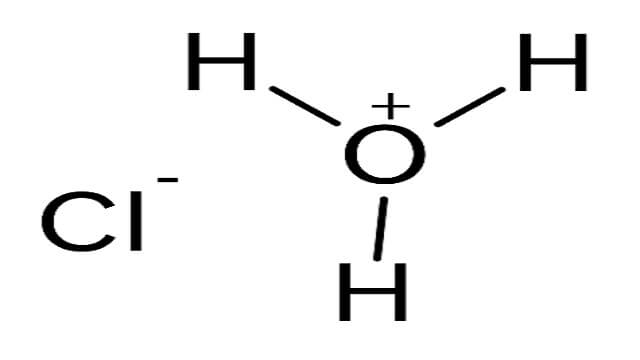
کاملا در آب محلول است و در صورت ترکیب با آب تجزیه می شود و هیدروژن خود را در محیط آزاد می کند و در نتیجه آن +H3O و –Cl تولید می شود و واکنش آن با آب بسیار گرمازا است.
خواص فیزیکی و شیمیایی
ویژگی های فیزیکی این ماده به غلظت آن بستگی دارد. با توجه به این امر برخی از ویژگی های اسید کلریدریک 37% در جدول زیر آورده شده است:
| فرمول شیمیایی | HCl |
| cas no | 7647-01-0 |
| جرم مولکولی | 36/46 g/mol |
| شکل ظاهری | مایع شفاف بی رنگ با بوی تیز |
| چگالی | 1/18 kg/L |
| نقطه ذوب | 30ºC- |
| نقطه جوش | 61ºC |
| pH | 1/1- |
روش تولید اسید کلریدریک
برای تولید این اسید قوی و خورنده روش های متعددی وجود دارد. در گذشته این ترکیب را از واکنش سدیم کلرید و اسید سولفوریک با نسبت مولی 2 به 1 تولید می کردند. معادله واکنش آن به صورت زیر است. همانطور که مشاهده می شود در این واکنش یک اسید معدنی با مقدار 2 برابر نمک سدیم کلرید ترکیب شده و در نتیجه آن هیدروکلریک اسید و سدیم سولفات تولید می شود.
2NaCl + H2SO4 → 2HCl + Na2SO4
روش های دیگری نیز برای تولید این ماده است، از طریق دیگر مواد شیمیایی مانند فرآیند کلروآلکالی تولید می شود. در نتیجه این فرآیند هیدروکسید، هیدروژن و کلرین ایجاد می شود که در ادامه با هم ترکیب شده و HCl تولید می کنند.
اسید کلریدریک چه کاربردی دارد؟
HCl یک اسید قوی معدنی است که کاربردهای صنعتی بسیاری از جمله پالایش فلزات دارد. کاربرد آن اغلب کیفیت محصول را تعیین می کند. هیدروژن کلرید در شیمی آلی برای تولید وینیل کلرید و دی کلرو اتان استفاده می شود. همچنین با آمینو تری متیلن فسفونیک اسید می تواند از تشکیل رسوب جلوگیری کند. در ادامه برخی از ویژگی های این ترکیب بیان شده است.
خالص سازی فولاد
یکی از مهمترین کاربردهای این اسید در خالص سازی و حذف ناخالصی های فولاد، حذف زنگ زدگی یا رسوبات اکسید آهن از آهن یا فولاد قبل از پردازش بعدی، مانند اکستروژن، نورد، گالوانیزه کردن و سایر تکنیک ها است. به طور تکنیکی از HCl 18% برای این فرآیند استفاده می شود.
Fe3O4 + Fe + 8HCl → 4FeCl2 + 4H2O
از اسید استفاده شده دوباره از محلول آهن کلرید بازیافت می شود، اما سطوج بالایی فلزات سنگین در اثر پالایش کاهش داده می شود.
تولید ترکیبات معدنی
مشابه استفاده از آن برای خالص سازی، اسید هیدروکلریک برای حل کردن بسیاری از فلزات، اکسیدهای فلزی و کربنات های فلزی استفاده می شود. معادله واکنش آن به صورت زیر نشان داده می شود:
Zn + 2HCl → ZnCl2 + H2
NiO + 2HCl → NiCl2 + H2O
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
کنترل pH و خنثی سازی
از این اسید جهت تنظیم pH محلول ها استفاده می شود. چرا که می تواند با هیدروکسید واکنش داده و آب و یون کلرید تولید کند. در صنایعی که به خلوص بالایی نیاز دارند (مانند صنایع غذایی، دارویی و آب آشامیدنی)، از هیدروکلریک اسید با کیفیت بالا برای کنترل اسیدیته جریان های آب استفاده می شود. در صنایع کم تقاضا، از اسیدهای با خلوص صنعتی برای خنثی کردن پساب ها و اسیدیته استخرها کافی است.
بازیافت رزین های تبادل یون
از HCl با کیفیت بالا به منظور بازسازی دوباره رزین های تبادل یونی استفاده می کنند. رزین های تبادل کاتیون به طور گسترده ای برای حذف یون هایی مانند سدیم و کلسیم از محلول های آبی و تولید آب های بدون ترکیبات معدنی استفاده می شوند.

از اسید برای جداسازی کاتیون ها از رزین استفاده می شود و در این فرآیند جای سدیم در رزین با هیدروژن پر می شود.
کاربردهای آزمایشگاهی
از شش اسید معدنی قوی رایج در شیمی، اسید هیدروکلریک اسیدی است که کمترین احتمال را دارد که تحت یک واکنش تداخلی اکسیداسیون کاهش قرار گیرد. این یکی از کم خطرترین اسیدهای قوی برای استفاده و نگهداری است. با وجود قدرت اسیدی زیاد، حاوی یون کلرید غیر سمی است. محلول های اسید کلریدریک با قدرت اسیدی متوسط پس از ذخیره سازی کاملاً پایدار هستند و غلظت خود را در طول زمان حفظ می کنند. این ویژگی ها، به علاوه این واقعیت که به عنوان یک معرف خالص در دسترس است، این ترکیب را به یک معرف اسیدی عالی تبدیل می کند. هیدروکلریک اسید ترجیحا در تیتراسیون برای تعیین مقدار بازها استفاده می شود. تیترهای اسیدی قوی به دلیل نقطه پایانی متمایزتر، نتایج دقیق تری ارائه می دهند.
سایر کاربردها
علاوه بر کاربردهای بالا این ماده در صنایع مختلف دیگری نیز مورد استفاده قرار می گیرد.
- چرم سازی
- تولید پاک کننده های خانگی (البته این روزها جایگزین این ماده برای این کاربرد، اسید سولفامیک است؛ برای خرید اسید سولفامیک با بهترین کیفیت و قیمت از شیمی استور)
- ساخت و ساز ساختمان
- حضور در واکنش تولید باریم کلرید (خرید باریم کلرید)
- تولید نفت (رایج ترین روش برای استخراج نفت دریای شمال)
- برای حل کردن کربنات کلسیم استفاده می شود. در مواردی مانند رسوب زدایی کتری و تمیز کردن ملات از روی آجر کاری می تواند مفید باشد.
- بسیاری از مواد غذایی از این ترکیب در ساختار خود استفاده می کنند. محصولاتی مانند آسپارتام، فروکتوز، اسید سیتریک (خرید اسید سیتریک)، لیزین، پروتئین گیاهی و ژلاتین دارای این ترکیب هستند.
همچنین از این ترکیب در تهیه شکل هیدراته کلرید روی نیز بهره می برند؛ برای خرید کلرید روی با کیفیت و قیمت مناسب با کارشناسان ما در شیمی استور تماس بگیرید.
تفاوت هیدروکلریک اسید و اسید کلریدریک چیست؟
اسید کلریدریک به HCl خالص اطلاق می شود اما هیدروکلریک اسید به محلول آبی HCl گفته می شود که دارای غلظت های متفاوتی است و فرمول آن به صورت H3OCl است. این ترکیب متناسب با غلظتی که دارد کاربردهای متفاوتی در صنعت خواهد داشت.
خطرات و MSDS اسید کلریدریک
همانطور که گفته شد HCl در دسته اسیدهای معدنی بسیار قوی قرار دارد و به شدت خورنده است. بنابراین هنگام کار با این ماده باید نکات ایمنی شامل استفاده از دستکش نیتریل دار، عینک و روپوش باید رعایت شود. همچنین برای جلوگیری از استشمام بخارات آن باید از ماسک استفاده شود. خاصیت خورندگی آن باعث شده بتواند به پوست (اورگان های زنده) و بسیاری از مواد آسیب وارد کند و تنها ماده ای که سالم می ماند پلاستیک است. به همین علت معمولاً هنگام کار با محلولهای غلیظ از دستکشهای محافظ لاستیکی و تجهیزات حفاظتی مربوطه استفاده میشود.
محلول10-25% آن موجب آسیب جدی به پوست و چشم می شود. در غظت های بیشتر از 10% موجب تولید گازهای کلر دار و تحریک دستگاه تنفسی شود. غلظت های بیشتر از 25% سوختگی شدید پوست و چشم را در پی دارد. در صورت تماس با پوست و چشم محل تماس را با آب سرد فراوان شسته و سریعا به پزشک مراجعه شود. در صورت بلع، دهان را با آب سرد و فراوان شسته و به سرعت به مرکز پزشکی مراجعه شود.
سوالات متداول
نقش هیدروکلریک اسید در معده چیست؟
این اسید که به اسید معده معروف است به هضم غذا و ایمنی بدن کمک می کند. این ترکیب به تجزیه پروتئین ها و جذب مواد مغذی کمک و ویروس ها و باکتری ها را کنترل می کند.
آیا اسید کلریدریک برای انسان ها مضر است؟
این ماده یک اسید بسیار قوی است و در تماس با پوست باعث سوختگی جدی می شود؛ همچنین تماس این ماده با چشم باعث کوری می شود. میزان آسیب و سوختگی ناشی از این ترکیب به غلظت آن بستگی دارد.
آیا اسید کلریدریک خوراکی است؟
خیر. بلع این ماده باعث درد، اسهال، استفراغ و حالت تهوع می شود؛ همچنین سوختگی دهان، گلو، معده و سایر اعضای داخلی بدن را به دنبال دارد.


























نجاتی –
آیا هیدروکلریک اسید همان هیپوکلرو اسید است؟
شیلا عقیلی –
خیر. فرمول شیمیایی هیدروکلریک اسید HCl و فرمول شیمیایی هیپوکلرو اسید HClO است.