اسید نیتریک (Nitric acid) ترکیبی بسیار خورنده با فرمول شیمیایی HNO3 است که به صورت مایع بی رنگ با بوی تند وجود دارد. عمده کاربرد این ترکیب در تولید کودها و مواد منفجره است. قرارگیری در معرض این ماده باعث تحریک چشم، پوست و غشای مخاطی می شود. اسید نیتریک در بازار عمدتا با غلظت 68% موجود است و به فروش می رسد. برای خرید این اسید با نازلترین قیمت به سایت شیمی استور مراجعه فرمایید.
قیمت خرید اسید نیتریک:
برای خرید این اسید و سایر ترکیبات شیمیایی به سایت شیمی استور مراجعه فرمایید. شیمی استور ارائه دهنده ی محصولات شیمیایی با بهترین کیفیت و نازلترین قیمت است.
نیتریک اسید چیست؟
اسید نیتریک (Nitric acid) با فرمول شیمیایی HNO3 و نام های دیگر تیزاب و جوهر شوره، یک اسید معدنی با خاصیت خورندگی بالا است. به صورت مایع ای بی رنگ با بخارهای زرد و بوی تند وجود دارد؛ اما به دلیل تجزیه این اسید پس از مدتی به رنگ زرد بدل می شود. این ترکیب بسیار خورنده و سمی است و باعث سوختگی شدید پوست می شود. به عنوان یک عامل اکسید کننده قوی، معرف رایج در آزمایشگاه ها، تولید مواد منفجره و کودها کاربرد دارد. این ماده اسیدی قوی است؛ زیرا هر چه اسید در محلول آبی بیشتر تفکیک شود آن اسید در گروه ترکیبات قوی قرار می گیرد. این ماده با شکستن یون هیدروژن و یون نیترات در آب کاملاً تجزیه می شود.
نیتریک اسید خوراکی:
شکل خوراکی این اسید در صنایع غذایی کاربرد دارد. در این صنعت از این ماده در پیشگیری از رشد باکتری ها، تثبیت رنگ گوشت قرمز و به عنوان نگهدارنده استفاده می کنند. این ترکیب یک ماده ی موثر در نگهداری محصولات گوشتی مانند سوسیس، کالباس، همبرگر و غیره است.

در برخی موارد اگر رنگ گوشت خریداری شده خیلی قرمز باشد به دلیل افزودن مقدار زیاد این اسید به گوشت است.
مشخصات فیزیکی و شیمیایی:
| ساختار | 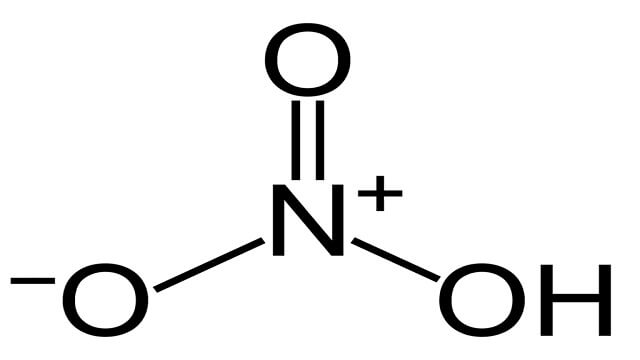 |
| نام دیگر | تیزاب، جوهر شوره |
| CAS NO | 7697-37-2 |
| فرمول شیمیایی | HNO3 |
| جرم مولکولی | 63.012 g/mol |
| مشخصات ظاهری | مایع بی رنگ با بوی تند |
| دانیسته | 1.51 g/cm3 |
| نقطه جوش | 83ºC |
| نقطه ذوب | 42ºC- |
| حلالیت | قابل اختلاط در آب |
| pH | 3.01 |
روش تولید:
این ماده را از واکنش دی اکسید نیتروژن با آب می سازند و فرمول آن به شرح زیر است:
NO2+2H2O→2HNO3+NO+NO2+H2O4
واکنش خالص به صورت:
NO2+H2O→2HNO3+NO3
معمولا اسید تولیدی توسط واکنش، توسط اکسیژن هوا برای تولید دی اکسید N2 اضافی دوباره اکسید می شود. حباب دی اکسید نیتروژن از طریق پراکسید هیدروژن می تواند به بهبود عملکرد اسید کمک کند.
2NO2+H2O2→2HNO3
روش تولید آزمایشگاهی:
معمولا اسیدی که فراریت بالاتری دارد را با اسیدی که فراریت کمتری دارد از نمک خود جدا می کنند و این موضوع یک اصل اساسی در تهیه آزمایشگاهی این ماده است. اسید نیتریک از اسید سولفوریک فرارتر است، از این رو توسط اسید سولفوریک از نیترات های فلزی جدا می شود. برای تولید آزمایشگاهی این محصول 50 گرم نیترات پتاسیم را به همراه 25 میلی لیتر اسید سولفوریک غلیظ در یک فلاسک ته گرد می ریزند و آن را تا 200 درجه سانتی گراد گرم می کنند و معادله ی این واکنش عبارت اند از:
KNO3+H2SO4 → KHSO4+HNO3
در روشی دیگر در آزمایشگاه ها این اسید را می توان از تجزیه حرارتی نیترات مس نیز تولید کرد. در اینجا دی اکسید نیتروژن و گازهای اکسیژن را تولید کرده و در ادامه از آب عبور می دهند. معادله این واکنش به شرح زیر است:
2Cu(NO3)2→2CuO+4NO2+O2
در ادامه فرایند استوالد:
2NO2+H2O→HNO2+HNO3
روش دیگر شامل واکنش بین مول های مساوی از هر نمک نیتراتی مانند نیترات سدیم با اسید سولفوریک و تقطیر این مخلوط در نقطه جوش این اسید در 83 درجه سانتی گراد است.
واکنش ها:
واکنش اسید نیتریک با پتاسیم سولفیت که باعث تولید پتاسیم سولفات می شود. البته دیگر فراورده های این واکنش نیتروژن دی اکسید و آب هستند.
کاربردهای اسید نیتریک:
از کاربردهای این ماده می توان به:
- تولید نیترات آمونیوم برای تولید پلاستیک، رنگ و کود
- ساخت مواد منفجره مانند TNT
- موشک های سوخت مایع به عنوان اکسید کننده
- شکل خالص برای حذف زگیل
- پیش ساز ترکیبات نیتروژن آلی
- پردازش فلزات
- نجاری
- پاک کننده ها
اشاره نمود. البته در صنعت پلیمر نیز می توان آن را دید.
تولید کود:
شاید اصلی ترین و عمده ترین کاربرد این ماده را بتوان تولید کود دانست. این اسید با آمونیاک خنثی می شود و نیترات آمونیوم را می سازد.

به طور کلی در تولید کودهای نیترات آمونیوم، کلسیم آمونیوم نیترات و اوره آمونیوم نیترات نیز کاربرد دارد.
سوخت موشک:
در موشک هایی که با سوخت مایع کار می کنند این اسید به عنوان اکسید کننده حضور و کاربرد دارد. شکل های مختلف این ماده به عنوان اکسید کننده شامل اسید نیتریک بخاردار قرمز و سفید، مخلوط با اسید سولفوریک است و به عنوان یکی از سه جزء سوخت مایع برای موشک ها به مصرف می رسند.
پردازش فلزات:
در فرایند تبدیل فلزات به اشکال اکسید شده ی آنها این ماده حضور دارد. برای مثال به راحتی می تواند فلز مس را به نیترات مس تبدیل کند. از سوی دیگر در ترکیب با اسید هیدروکلریک به منظور انحلال فلزات نجیب استفاده می شود. این توانایی این ماده در انحلال انتخابی فلزات در فرایندهای جداسازی طلا بسیار مفید و موثر است.
نجاری:
در غلظت های کم، اسید نیتریک اغلب برای ایجاد کهنگی مصنوعی کاج و افرا کاربرد دارد. همچنین رنگ تولید شده طلایی خاکستری است که بسیار شبیه به چوب قدیمی مومی یا روغنی است.
ترکیبات پاک کننده:
خاصیت خورندگی این ماده برای برخی کاربردهای تخصصی مانند:
- حکاکی در چاپ
- ترشی فولاد ضد زنگ
- تمیز کردن ویفرهای سیلیکونی در الکترونیک
استفاده می شود. این اسید در ترکیب با اسید کلریدریک یا به تنهایی در تمیز کردن پوشش شیشه ای و لام های شیشه ای مورد استفاده در کاربردهای میکروسکوپی، استفاده می شود. همچنین برای تمیز کردن شیشه پیش از نقره کاری در زمان ساخت آینه های نقره کاربرد دارد.
بازار جهانی:
ارزش بازار جهانی این ماده 29.8 میلیارد دلار در سال 2022 بوده است و پیش بینی می شود رشد 2.4% را بین سال های 2023 تا 2030 داشته باشد. افزایش تولید این ماده به افزایش درخواست آن به کودها برمیگردد؛ زیرا در طیف گسترده ای از کودهای کشاورزی مانند آمونیوم نیترات،آمونیوم کلسیم نیترات و غیره حضور و کاربرد دارد. در سال 2022 تقریبا 80.53 درصد تولید جهانی این ماده در تولید کودها مصرف شد.
اسید نیتریک را از کجا بخریم؟
برای خرید این محصول و سایر ترکیبات شیمیایی به سایت شیمی استور مراجعه فرمایید. شیمی استور ارائه دهنده ی محصولات شیمیایی با بهترین کیفیت و قیمت است.
MSDS و نکات ایمنی:
این اسید ترکیبی خطرناک، قابل اشتعال و خورنده است و بهتر است پیش از کار با آن برگه اطلاعات ایمنی مربوط به آن را مطالعه کنید.
- در زمان کار از لباس، عینک و دستکش محافظ استفاده کنید.
- حتما در محیطی باز یا دارای تهویه با آن کار کنید.
- پس از استنشاق، محیط کار را ترک و هوای تازه استشمام کنید.
- در صورت بلع تصادفی دهان را با آب بشویید و سعی نکنید با استفراغ آن را خارج کنید.
- پس از تماس با پوست، فورا لباس ها را تعویض کرده و آن ناحیه را برای 15 دقیقه با آب فراوان بشویید.
- در صورت تماس با چشم برای 15دقیقه با آب فراوان چشم آسیب دیده را بشویید و لنز تماسی را خارج کنید و شستشو را ادامه دهید.
- برای خاموش کردن آتش از کربن دی اکسید، مواد شیمیایی خشک یا کف های خاموش کننده استفاده کنید.
- این ترکیب را در ظرف در بسته در محیطی خشک و دارای تهویه نگهداری کنید.
با رعایت نکات ایمنی خطرات ناشی از کار با این ماده را کاهش دهید.
جمع بندی:
اسید نیتریک یا جوهر شوره یک ترکیبی معدنی است که عمده کاربرد آن در تولید کودها و مواد منفجره است. روش های متنوعی برای تولید آن وجود دارد و می توان در آزمایشگاه ها نیز آن را به کار برد. برای خرید نیتریک اسید با بهترین کیفیت و قیمت به سایت شیمی استور مراجعه فرمایید.



























محمود اکبری –
سلام. گالن ۲۰لیتری اسید نیتریک درصد خلوصش چقدره؟
شیلا عقیلی –
سلام، بر طبق آنالیز موجود در سایت خلوص اسید نیتریک 53% است.
سهرابی –
از اسید نیتریک در تولید کود هم کاربرد استفاده میشه؟
شیلا عقیلی –
بله، از این ماده در تولید کودهای شیمیایی جهت تهیه نیترات های پتاسیم، سدیم، آمونیوم و کلسیم استفاده می کنند. این ماده با اکسیده شدن آمونیاک و اکسیداسیون نیتروژن نیترات را می سازد.