ترکیبی شیمیایی است که در دسته اسید های کربوکسیلیک ساده قرار می گیرد، اسید بنزوئیک (benzoic acid) نام دارد. مولکول بنزوئیک اسید (به ویژه حلقه بنزن) غیرقطبی و در نتیجه آبگریز است.ساختار اسید بنزوئیک شامل یک مولکول بنزن است که به یک کربوکسیلیک اسید متصل شده است. به همین جهت آن را با نام کربوکسی بنزن نیز می شناسند. این ماده نقش آنتی میکروبی و نگهدارنده مواد غذایی، بازدارنده (تریاسیل گلیسرول لیپاز)، متابولیت گیاهی و یک آلرژن دارویی است. این ترکیب اسید مزدوج بنزوات است و اولین بار در قرن شانزدهم کشف شد. اولین بار تقطیر خشک صمغ اسید بنزوئیک در سال 1556 توسط نوستراداموس، در سال 1560 توسط پدمونتانا و در سال 1596 ویگنر شرح داده شد.
خرید:
برای خرید اسید بنزوئیک با قیمت مناسب و کیفیت عالی با کارشناسان ما در واحد فروش تماس بگیرید.
خواص فیزیکی و شیمیایی
این ترکیب به صورت پودر کریستالی بی رنگ و با بویی ضعیف و مطبوع است. ساختار کریستالی مونو کلینیک مسطح دارد. نام آیوپاک آن بنزن کربوکسیلیک اسید است.
| ساختار | 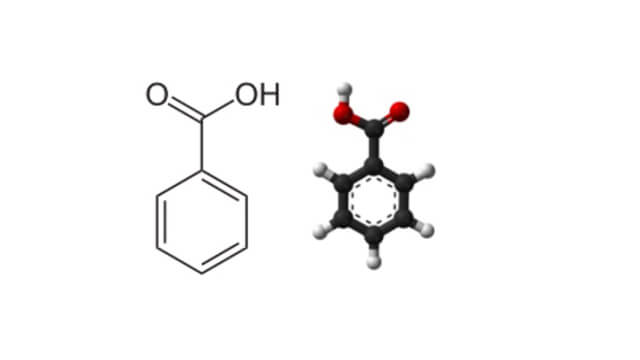 |
| فرمول شیمیایی | C7H6O2 |
| cas no | 65-85-0 |
| جرم مولکولی | 122.123 g/mol |
| شکل ظاهری | کریستال های بی رنگ با بویی ضعیف و مطبوع |
| دانسیته (15 درجه سانتیگراد) | 1.26 g/ml |
| نقطه ذوب | 122ºC |
| نقطه جوش | 250ºC |
| اسیدیته (در آب) | 4.20 |
| حلالیت | محلول در استون، بنزن، الکل، هگزان و استات ها |
روش تولید اسید بنزوئیک
این ترکیب را می توان به طور طبیعی در میوه هایی مانند توت فرنگی، آلو خشک و سیب وجود دارد. همچنین لبینات هایی مانند ماست نیز حاوی این ترکیب است.
سنتز بنزوئیک اسید از تولوئن
این ماده به صورت تجاری از واکنش اکسایش جزئی تولوئن در حضور اکسیژن تولید می شود. این فرآیند در حضور کاتالیزور کبالت یا منگنز نفتنات انجام می شود. معادله این واکنش به صورت تصویر زیر است:
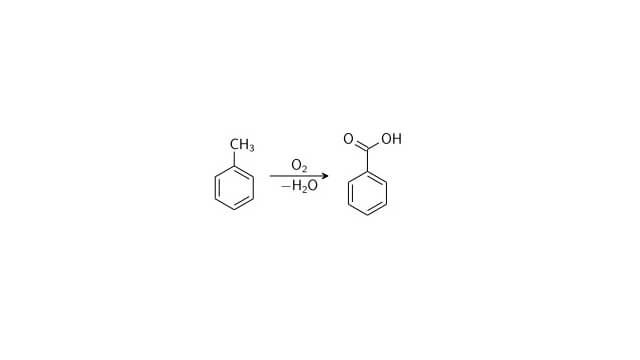
در روشی دیگر از واکنش بنزو تری آزول با هیدروکسید کلسیم در آب با کمک کاتالیزور آهن یا نمک های آهن استفاده می شود.
سنتز آزمایشگاهی
ایبن ترکیب ماده ای ارزان و در دسترس است، به همین دلیل سنتز آزمایشگاهی آن عمدتا با اهداف آموزشی انجام می شود. این ترکیب را می توان با تبلور مجدد در آب، خالص کرد زیرا در آب گرم محلول و در آب سرد کم محلول است. عدم استفاده از حلال های سمی، باعث خنثی سازی ایمن این ماده می شود و مقدار بازدهی این فرآیند 65% است.
هیدرولیز
مانند دیگر نیتریل ها و آمیدها، بنزو نیتریل و بنزآمید را می توان در شرایط اسیدی یا بازی به این ترکیب یا باز مزدوج آن هیدرولیز کرد.
معرف گرینیارد
برمو بنزن را می توان با کربوکسیلاسیون حدواسط فنیل منیزیم برمید به اسید بنزوئیک تبدیل کرد. این روش یک آزمایش جذاب برای نشان دادن واکنش گرینیارد به دانشجویان است.
اکسیداسیون ترکیبات بنزیلی
بنزیل الکل و بنزیل کلراید و تمامی مشتقات بنزیل می توانند طی واکنش اکسیداسیون به این ترکیب تبدیل شوند.
واکنش های اسید بنزوئیک
در ادامه برخی از واکنش های این ترکیب را بررسی خواهیم کرد.
واکنش در حلقه آروماتیک
جانشینی الکتروفیلی آروماتیک می تواند در سه موقعیت صورت بگیرد که با توجه به وجود گروه کربوکسیلیک اسید در یکی از موقعیت ها، الکتروفیل می تواند در دو موقعیت دیگر متا نسبت به گروه عاملی قرار بگیرند.
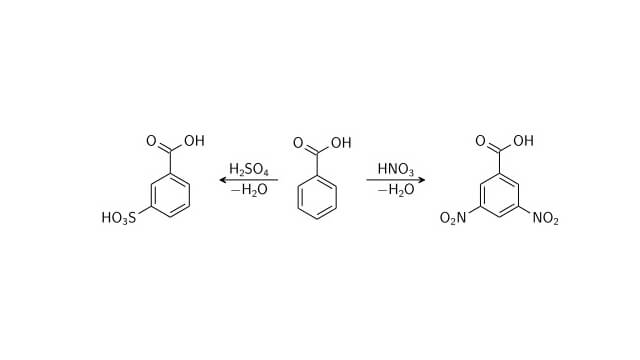
واکنش در گروه کربوکسیل
در گروه کربوکسیل واکنش ها شامل موارد زیادی می شود که در ادامه به آن ها اشاره خواهیم کرد:
- استرهای بنزوات محصول واکنش اسید کاتالیز شده با الکل ها هستند.
- آمیدهای اسید بنزوئیک معمولاً از بنزوئیل کلرید تهیه می شوند.
- دهیدراسیون بنزوئیک انیدرید با اسیتیک انیدرید یا پنتوکسید فسفر صورت می گیرد.
- مشتقات اسیدی بسیار فعال مانند هالیدهای اسید به راحتی با مخلوط کردن با عوامل هالوژناسیون مانند کلریدهای فسفر یا تیونیل کلراید به دست می آیند.
- ارتواسترها را می توان با واکنش الکل ها در شرایط بدون آب اسیدی با بنزونیتریل به دست آورد.
- کاهش بنزآلدهید و بنزیل الکل با استفاده از DIBAL-H ، LiAlH4 یا سدیم بوروهیدرید امکان پذیر است.
همچنین دکربوکسیلاسیون به بنزن ممکن است با حرارت دادن در کینولین در حضور نمک های مس انجام شود.
کاربردهای اسید بنزوئیک
اسید بنزوئیک عمدتا در تولید فنل با دکربوکسیلاسیون اکسیداتیو در دمای 300-400 درجه سانتی گراد استفاده می شود. دمای لازم برای انجام این واکنش حدود 200 درجه سانتیگراد است که در صورتی که از نمک فلز مس به عنوان کاتالیزور انجام می گیرد.
2C6H5CO2H + O2 → 2C6H5OH + CO2
فنول را می توان به سیکلوهگزانول تبدیل کرد که خود این ماده نیز در سنتز نایلون استفاده می شود. همچنین با خالص سازی سدیم هیدروکسید به همراه این ماده می توان سدیم بنزوات را ساخت.
پیش ساز نرم کننده ها
نرم کننده های بنزوات مانند گلیکول، دی اتیل گلیکول و تری اتیل گلیکول استرها از واکنش ترنس استری شدن متیل بنزوات با دی ال مربوطه به دست می آیند. این نرم کننده ها که مانند استرهای ترفتالیک اسید استفاده می شود، جایگزین مناسبی برای فتالات ها هستند.
پیش ماده بنزوات سدیم و نگهدارنده های مرتبط
این ترکیب و نمک های آن به عنوان نگهدارنده مواد غذایی استفاده می شود. از رشد کپک، مخمر و برخی از باکتری ها جلوگیری می کند. این ماده یا به طور مستقیم به مواد غذایی اضافه می شود یا از واکنش با نمک سدیم، پتاسیم و کلسیم ایجاد می شود. در بسیاری از غذاها و نوشیدنی های اسیدی مانند آب میوه (حاوی اسید سیتریک)، نوشابه های گازدار (خرید اسید فسفریک)، ترشی ها (استیک اسید) و… به منظور تنظیم اسیدیته استفاده می شود. فعالیت ضد میکروبی آن در محدوده pH از 2.5 تا 4.0 خوب خواهد بود.
کاربرد در صنایع دارویی
اسید بنزوئیک برای پوست جهت درمان بیماری های قارچی پوست مانند قوزک، کرم حلقوی در ورزشکاران استفاده می شود. همچنین جز اصلی صمغ بنزوئین است و به عنوان مواد ضد عفونی کننده و ضد احتقانی استنشاقی استفاده می شود. از طرفی به عنوان یک ترکیب خلط آور، مسکن و ضدعفونی کننده استفاده می شود.
کاربرد در لوازم آرایشی
بنزوئیک اسید یک اسید آروماتیک است که در طیف گسترده ای از لوازم آرایشی به عنوان حلال، نرم کننده، تنظیم کننده pH و نگهدارنده استفاده می شود. این ماده سابقه طولانی استفاده به عنوان یک عامل ضد قارچی در آماده سازی های درمانی موضعی دارد.
ایمنی بنزیل الکل، بنزوئیک اسید، بنزوات سدیم، بنزوات کلسیم، بنزوات پتاسیم و بنزیل بنزوات توسط پنل تخصصی بررسی مواد آرایشی (CIR) ارزیابی شده است. پانل متخصص CIR داده های علمی را ارزیابی کرد و به این نتیجه رسید که این مواد برای استفاده در محصولات آرایشی بی خطر هستند.
کاربرد در صنایع رنگ
اسید بنزوئیک را می توان به عنوان یک نگهدارنده در فرمولاسیون امولسیونی شوینده های مایع، رنگ ها، پولیش ها و موم ها به عنوان عامل ضد رسوب و بازدارنده خوردگی، افزودنی رنگ و پوشش، عامل آبکاری، عامل تصفیه سطح (به ویژه در تولید فلز) و جهت افزایش پایداری ذخیره سازی استفاده کرد.
کاربرد در پلاستیک
بنزواتها نرمکنندههای حلالشونده جهت تولید PVC هستند که به صورت تکبنزوات یا دیبنزوات در دسترس هستند. آنها عمدتاً در تولید PVC از جمله کفپوش و فیلم و همچنین در چسب ها و درزگیرها استفاده می شوند.
خطرات، Msds و نکات ایمنی اسید بنزوئیک
این ترکیب اسیدی است و می تواند در تماس با پوست و چشم بسیار خورنده باشد و آسیب وارد کند. در هنگام کار با آن از دستکش و عینک ایمنی استفاده کنید.
- چشم: در برخورد با چشم باعث تحریک، قرمزی و درد می شود. چشم ها را به مدت 15 دقیقه با آب بشویید. به پزشک مراجعه کنید.
- پوست: در تماس با پوست، موجب تحریک آن می شود. اگر از طریق پوست جذب شود آسیب جدی وارد می کند. موجب قرمزی و التهاب پوست می شود. پوست به مدت 15 دقیقه با آب و صابون شسته شود و از کمک های اولیه استفاده کنید.
- بلع: اگر بلعیده شود می تواند موجب تحریک و درد و آسیب دستگاه گوارشی شود. دهان را تمیز بشویید و 3-4 لیوان آب یا شیر بنوشید. به پزشک مراجعه کنید.
- تنفس: اگر استنشاق شود، به شش ها آسیب می زند. اگر به طور متناوب به مدت 4 هفته در معرض غبار آن باشید دچار مشکل فیبروز بینابینی می شود. از هوای تازه استفاده کنید و در صورت مشکل در تنفس، از اکسیژن استفاده کنید و به پزشک مراجعه کنید.
با رعایت نکات ایمنی خطرات ناشی از کار با این ماده ی شیمیایی را کاهش دهید.
جمع بندی:
یک ترکیب شیمیایی که در دسته ی اسید های کربوکسیلیک قرار دارد، اسید بنزوئیک نام دارد. این ماده با فرمول شیمیایی C7H6O2 در آب کم محلول و در سایر ترکیبات از جمله استون، الکل، هگزان و غیره محلول است. این اسید خطرناک و خورنده کاربردهای بسیاری در صنایع مختلف دارد.
سوالات متداول
آیا اسید بنزوئیک در آب محلول است؟
مقدار حلالیت این ماده در آب، در دما های مختلف متفاومت است. برای مثال در دمای صفر درجه مقدار 1.7 گرم بر یک لیتر آب و در دمای 100 درجه سانتی گراد مقدار 56.3 گرم از آن در یک لیتر آب حل می شود.
اسید بنزوئیک برای پوست ایمن است؟
در محصولات آرایشی و مراقبت پوستی از غلظت 5% اسید بنزوئیک استفاده می کنند که این مقدار در این محصولات ایمن و بی خطر است.
بنزوئیک اسید چند پیوند یگانه دارد؟
با توجه به فرمول ساختاری آن، این ماده دارای 4 پیوند یگانه است.
اسید بنزوئیک اسید قوی است یا ضعیف؟
این ماده یک اسید ضعیف است.























سهرابی –
مقدار مجاز اسید بنزوئیک در مواد غذایی چقدر است؟
شیلا عقیلی –
مقدار مجاز این ماده در مواد غذایی 0.5 تا 0.2 درصد است